问题进行探究。
一、“软硬酸碱”的定义
软硬酸碱理论Hard and Soft Acids and Bases核心是根据酸碱的“硬度”()与“软度”()分类,解释和预测化合物的稳定性、反应活性及化学键类型上的局限性。
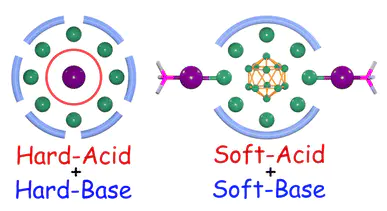
10.1039/d3dt02387g
硬酸的本质是电子对接受体的“硬”,这源于电子云的“刚性”。硬酸的电子云难以被外界电场(如碱的孤对电子)极化,其成键时倾向于形成离子键或极性共价键。
阳离子半径小电荷高极化性低软酸(Soft Acids)
软酸具有、、等特点,其价层电子受核束缚弱,电子云流动性强。
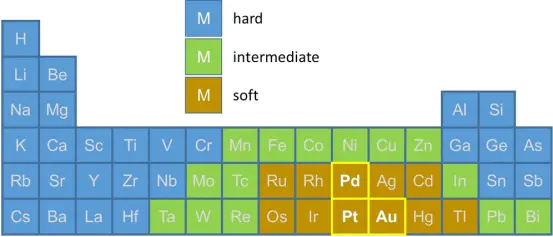
DOI: 10.1002/tcr.202300148
硬碱的本质是电子对给予体的“硬”,具体表现为硬碱孤对电子的“稳定性”。硬碱的孤对电子不易被酸的正电荷极化,成键时优先与硬酸形成稳定作用。
阴离子半径小电负性高极化性低DOI: 10.1016/S1386-1425(02)00230-5
软碱的本质是电子对给予体的“软”,具体表现为软碱孤对电子易被酸的正电荷极化,成键时优先与硬酸形成稳定作用。
阴离子半径大电负性低极化性高DOI: 10.1021/acs.cgd.6b01408
其性质介于硬酸碱与软酸碱之间例如,2+作为交界酸,可与硬碱–形成2沉淀,也能与软碱–形成稳定的64-配离子;交界碱2–,既可以和硬酸结合形成不稳定的HNO2,也能与软酸+形成配位能力较强的配合物。
DOI: 10.1002/ejic.202000423
二、软硬酸碱的作用规律
当硬酸与硬碱结合时,形成离子键或强极性共价键当软酸与软碱结合时,形成共价键(或配位键)当硬酸与软碱、软酸与硬碱结合时,形成的化合物稳定性差,易分解或发生配体取代反应;当交界酸碱结合时,其稳定性中等,需结合溶剂、温度等具体环境判断,反应选择性较弱。
2. 反应选择性
一方面,竞争反应中酸碱会优先与“同类” 结合FIFHFIAgI另一方面,配体取代反应的方向呈现出明显规律,硬酸的配合物中,硬碱配体易被其他硬碱取代、软碱配体难以取代,软酸的配合物则相反[Fe (H₂O)₆]–OIDOI: 10.1002/ajoc.201800069
硬溶剂(如2、甲醇)倾向于通过氢键或离子–偶极作用溶剂化硬酸碱,降低其反应活性。
硬硬反应在软溶剂中更易发生,软–软反应在硬溶剂中更易发生DOI: 10.1039/D0CY02011G
三、应用场景
,如硬酸2+、2+多与硬碱2-、32-形成碳酸盐、氧化物,软酸+、+多与软碱2-形成硫化物。
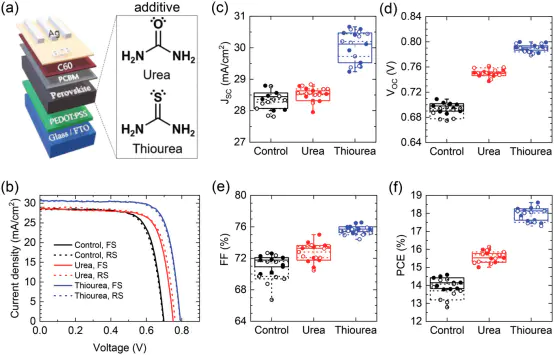
,例如硬酸3+与硬碱形成稳定配合物用于滴定分析,软酸Pt2+与软碱、CN–形成稳定配合物用于催化无机合成与分离提纯:软硬酸碱理论可指导合成路线设计–HF,利用软硬酸碱的选择性结合分离混合离子。
FeCuFeCl[FeCl]CuClCuC催化反应机理阐释:(如Pt(如烯烃的C=C键、CO的孤对电子)优先结合2+与烯烃配位,降低加氢反应的活化能。
在均相催化中,配体的软硬性质可调控催化活性DOI: 10.1002/anie.202414721
四、理论优势与局限性
软硬酸碱理论的优势在于其简洁性与广泛适用性。同时,其应用范围广,涵盖无机、有机、配位及生物化学等多个领域,能够合理解释离子键、共价键与配位键等多种键型的形成规律。实用性强,能够直接指导合成路径设计、分离方法开发、催化剂筛选以及药物分子设计等工作,有助于降低实验探索成本。
,其次该理论难以精确量化化合物的稳定性与反应速率,也未能充分考虑温度、压力、溶剂极性等外部条件对反应的影响,因此在处理“软硬交界”型体系时预测准确性有限。
DOI: 10.1021/acs.energyfuels.4c00817






