:是描述单位正电荷势能的标量场,源于与电子云的叠加贡献,具有保守场、可叠加性等特性,是连接微观电子结构与宏观相互作用的核心量。
DFT机器学习静电势()是描述静电场中单位正电荷所具有势能的标量场,其核心定义可通过电场强度的线积分表达。
在量子化学与分子模拟的框架下,静电势的物DOI:10.1016/j.rechem.2023.101046
间某点对带正电探针的吸引或排斥趋势——负值区域因电子云密度较高,对正电荷探针表现出较强吸引力,易与阳离子发生相互作用;正值区域则因核电荷暴露或电子云稀疏,对正电荷探针产生排斥,更易吸引阴离子。
这些特性使得静电势成为连接微观电子结构与宏观分子间相互作用的核心物理量作用。

静电势的计算方法随研究体系的尺度与复杂度发展出多套理论框架,涵盖量子化学精确计算、连续介质模型在量子化学框架下,密度泛函理论(DFT)Kohn-Shamρ(r),再基于ρ(r)计算静电势。
与电子密度泛函项为提升计算精度,广义梯度近似(GGA)泛函通过引入电子密度的梯度修正,比局域密度近似更准确地描述电子云的非均匀分布,尤其在分子界面或缺陷附近。
投影缀加波(PAW)这种方法在保留核心电子对静电势贡献的同时,大幅降低计算成本,适用于包含重元素的复杂体系。

针对生物大分子的溶液体系,连续介质模型Poisson-Boltzmann(ε(r)为提升求解效率,算法层面发展出自适应笛卡尔网格法,通过在分子界面处加密网格,在保证精度的同时减少计算量;快速多极子法(FMM)则通过将远场相互作用近似为多极子展开,将计算复杂度从O(N²)降至O(N),使核糖体等超大体系的静电势计算成为可能。
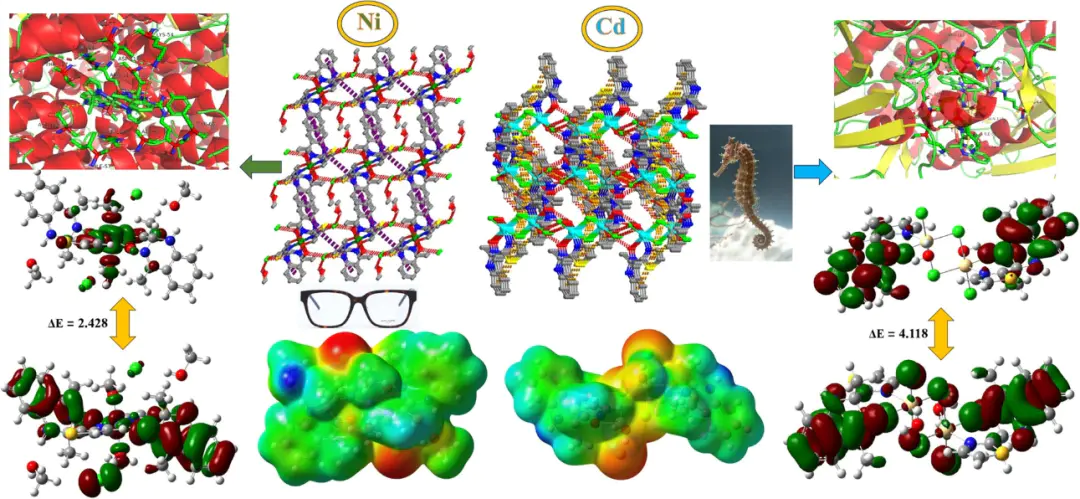
对于追求极致效率的高通量筛选(r-Rₐ)/|r-Rₐ|³+… )通过预存不同化学环境下原子的多极参数,可快速重建蛋白质等生物分子的静电势,计算速度比DFT快1-2个数量级,虽精度略有损失,但能满足大规模筛选需求。
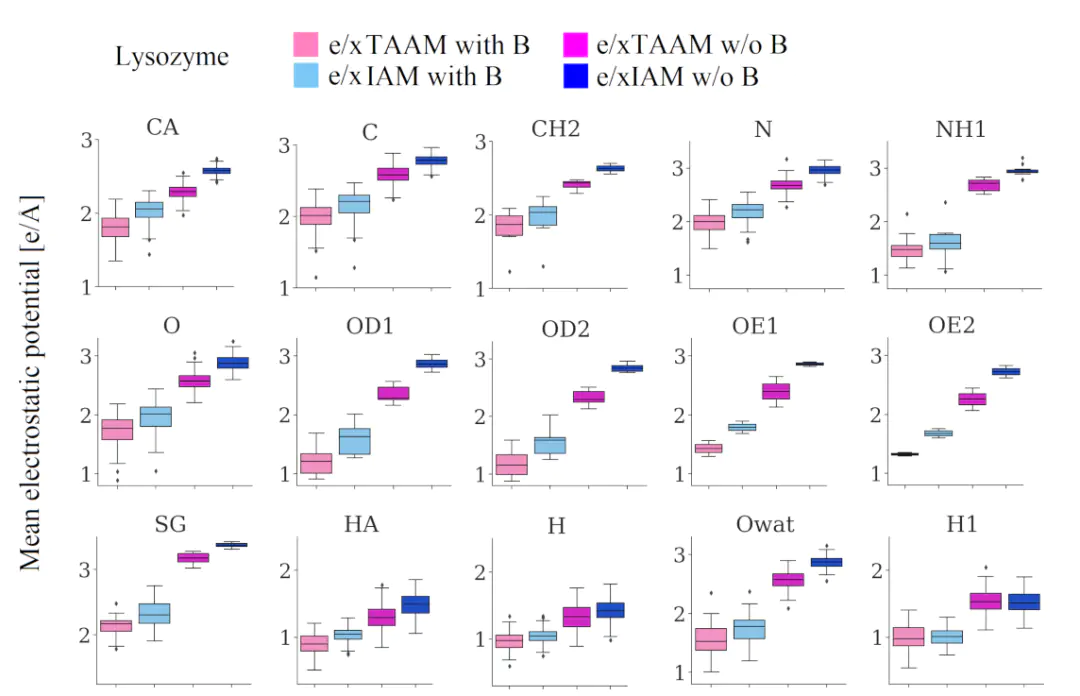
这些方法的协同应用,使得静电势计算能够覆盖从原子级电子结构到宏观生物体系的全尺度研究,为不同领域的理论分析提供灵活工具。
静电势前沿
机器学习驱动的静电势GNN其核心优势在于摆脱了传统量子化学计算对电子密度的依赖,通过训练集优化网络参数,预测速度较DFT计算提升100倍以上,且误差可控制在5%以内。这种方法特别适用于高通量筛选能,加速先导化合物的发现。
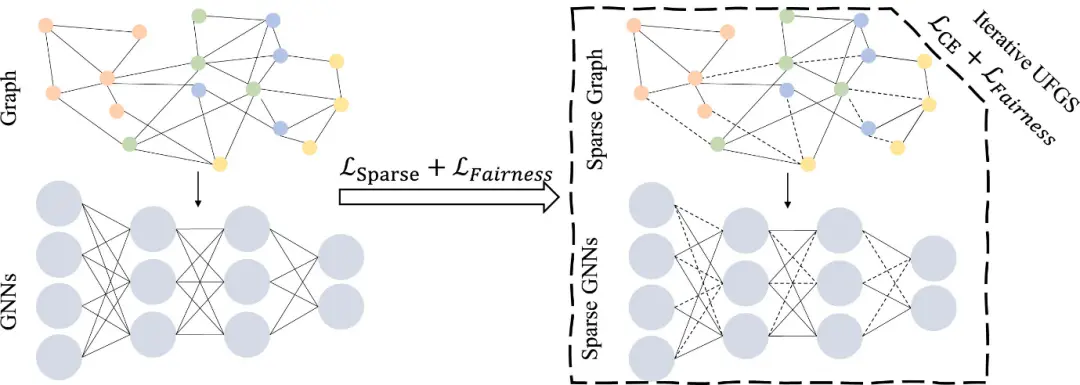
非局部介电响应理论则针对经典连PB新理论引入关联长度ξ描述这种非局部效应,这一修正显著改善了界面处静电势的计算精度,例如在DNA双链表面,非局部理论计算的静电势与实验测量的X射线散射数据吻合度比传统PB方程提高20%,更准确反映了溶剂化效应对静电势的调制。
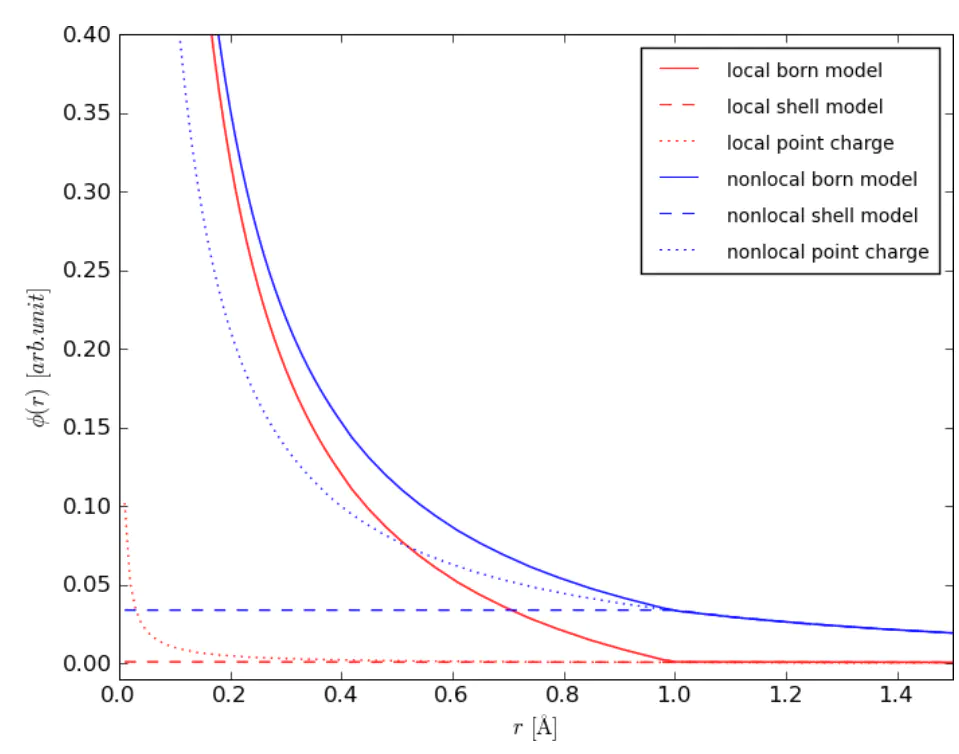
并行化计算技术DelPhiForce其核心机制是利用GPU的thousands of cores同时处理网格点的电势计算,将每步分子动力学例如,在肌球蛋白与肌动蛋白的相互作用模拟中,GPU加速的静电势计算揭示了构象变化如何通过改变表面电势分布调节结合强度,为肌肉收缩机制提供了新见解。
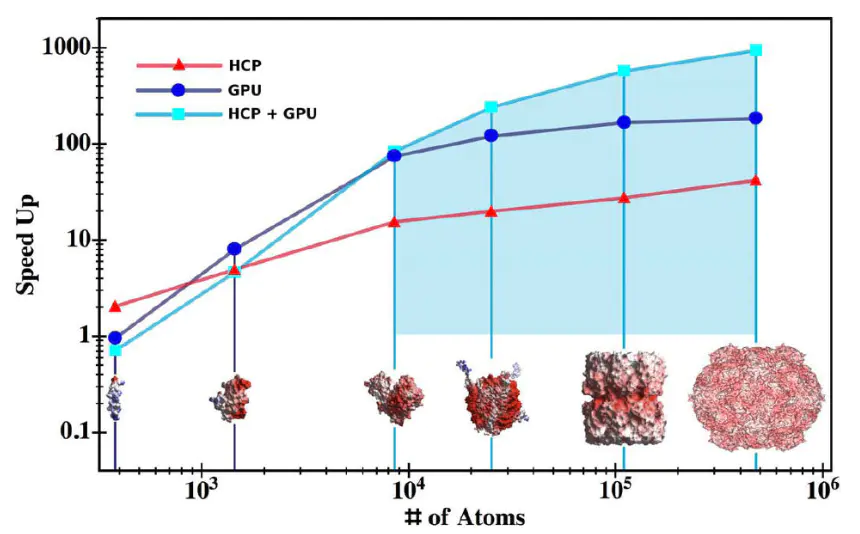
这些前沿进展不仅提升了静电势计算的性能,更拓展了其应用场景,使其从静态结构分析迈向动态功能解析,为复杂体系的理论研究提供了更强有力的工具。
微管静电势应用
Electrostatics of nanosystems: Application to microtubules》为例,理解细胞内物质运输的分子基础提供了关键理论依据。
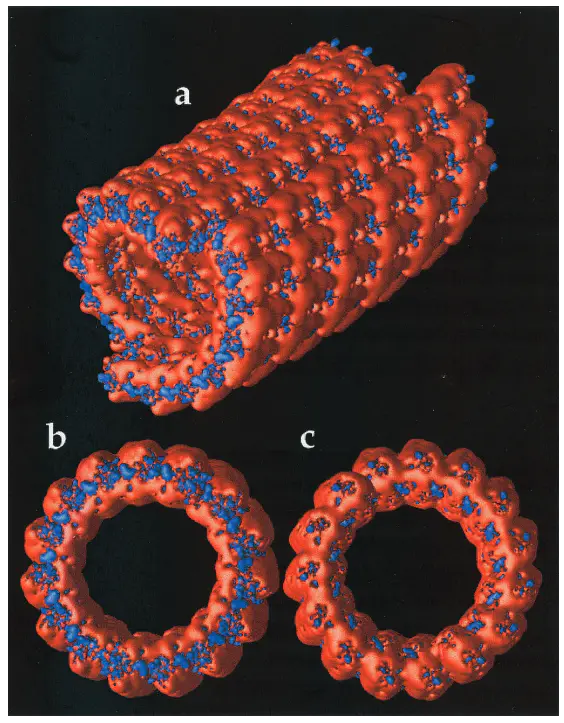
计算目标聚焦于微管这一细胞骨架的核心组件,其由α/β微管蛋白异二聚体纵向排列形成中空管状结构,直径约25 nm,长度可达微米级,是驱动蛋白沿其移动并运输囊泡的轨道,研究旨在通过静电势分布方法流程严谨且层次分明:首先进行结构准备,从数据库获取微管蛋白的晶体结构接着求解PB方程,使用APBS软件进行数值计算,网格参数设置为0.5 Å分辨率以确保界面处的计算精度,蛋白内部的介电常数设为2,溶剂区(水相)设为80,离子强度为150 mM,采用自适应有限差分法处理不规则的分子边界;最后通过可视化软件展示静电势等值面,其中蓝色代表负电势区域,红色代表正电势区域。
:微管外表面的深蓝区域对应强负电势,主要由β微管蛋白上的天冬氨酸、谷氨酸残基贡献,这种负电势可通过静电吸引与驱动蛋白的阳离子结构域结合,为驱动蛋白提供初始锚定位点,并指导其沿微管的运动方向。
——通过修饰微管表面的负电势区域,可干扰驱动蛋白的结合,抑制细胞分裂,为癌症治疗提供新策略。
DOI:10.1073/pnas.181342398
总结
从方法演化来看,静电势计算已形成多层次解决方案:量子化学框架下的与PAW方法提供原子级精度,适用于小分子、固体表面等体系的电子结构与静电势关联分析。
当前研究趋势聚焦于三个方向:其一,,图神经网络通过数据驱动的方式实现分子结构到静电势场的快速映射,将计算效率提升个数量级,同时保持与DFT相当的精度,为药物设计、材料筛选等领域的大规模应用其二,,通过引入空间色散效应修正传统方程在分子界面处的偏差,更准确描述氢键网络、溶剂化效应对静电势的调制,目前该理论已在蛋白–配体结合、膜蛋白功能等研究中展现出优势,未来需进一步拓展至复杂多相体系。
静电动态耦合机制,结GPU掌握静电势计算的核心模型与前沿工具,对于多个领域的理论研究具有不可替代的纳米材料设计酶催化机制解析药物开发,静efficacy随着理论方法的持续完善与计算能力的提升,静电势计算将在连接微观电子结构与宏观功能性能的研究中发挥更核心的作用,推动从理性设计到实际应用的高效转化。
评论列表