近年来,一种因新冠疫情而广为人知的技术-mRNA疫苗,正以其独特的机制和令人振奋的早期数据,为癌症治疗绘制出一幅充满希望的新蓝图。
关于mRNA癌症疫苗
传统的疫苗,如HPV疫苗,其作用是在疾病发生前,训练免疫系统识别并清除特定的病毒,从而阻断由病毒感染引发的癌症。而mRNA疫苗工作原理精巧而高效:mRNA疫苗的基本原理是将编码肿瘤抗原的mRNA导入体内,利用细胞内的翻译机制产生抗原蛋白,这些抗原蛋白降解后形成的抗原表位,通过MHC途径呈递给T细胞,从而激活免疫应答,达到治疗肿瘤的目的。mRNA疫苗具有无病毒成分、无感染风险、免疫原性强、研发周期短等优点,是未来肿瘤免疫治疗的重要方向。与传统疫苗相比,肿瘤mRNA疫苗具有无病毒成分、无感染风险、免疫原性强、研发周期短等显著优势,这为肿瘤的治疗提供了新的思路和方法。
图片来源于PENNLIVE patriot-News
新冠mRNA疫苗与癌症疫苗之间的关键区别之一是前者可以标准化并大规模生产,因为病毒靶标片段是相同的;而癌症疫苗则必须量身定制。每个肿瘤都有独特的基因图谱,因此个性化疫苗无法现成生产。
临床试验点燃实体瘤患者希望
理论令人振奋,数据则给予我们实实在在的信心。目前,全球已有超过120项mRNA癌症疫苗临床试验正在进行,覆盖肺癌、肝癌、胰腺癌、黑色素瘤等多种实体瘤,为患者带来了实实在在的生存获益。
黑色素瘤的重大突破
2026年1月,Moderna与默沙东联合公告:其个体化mRNA癌症疫苗V940(mRNA-4157)在针对高风险黑色素瘤的临床试验中,与PD-1抑制剂Keytruda联用,展现了惊人的效果。与单用Keytruda相比,联合疗法将患者的复发或死亡风险降低了49%。
头颈癌的新希望
德国BioNTech公司的mRNA疫苗BNT113,在治疗HPV16阳性头颈部鳞状细胞癌(HNSCC)的临床试验中也表现出色。2024年欧洲肿瘤内科学会(ESMO)上公布的数据显示,BNT113联合帕博利珠单抗,为患者带来了中位总生存期(OS)22.6个月的积极结果。该疫苗已获得美国FDA的快速通道资格,研发进程有望加快。
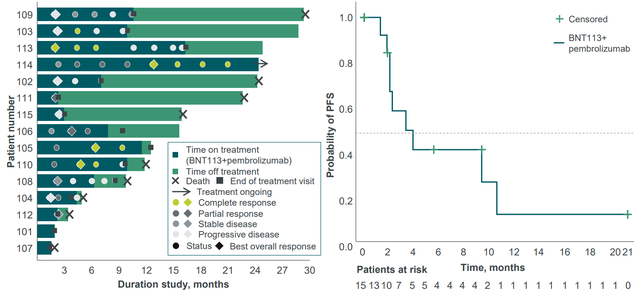
“癌王”胰腺癌的挑战与机遇
在生存率极低的胰腺癌领域,mRNA疫苗也初露锋芒。BioNTech的另一款个体化新抗原疫苗Autogene cevumeran(BNT122)的临床研究显示,在16例可评估患者中,8例产生了特异性T细胞反应。值得注意的是,产生免疫应答的8例患者在中位随访期后均未出现复发,而无应答患者的无复发生存期(RFS)为13.4个月,数据提示疫苗应答者疾病进展或死亡的风险显著降低。
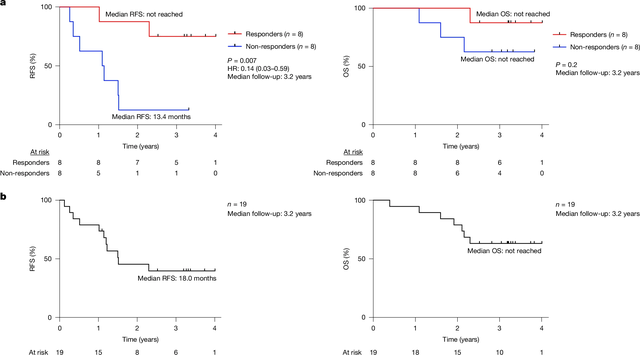
中国力量:本土创新加速追赶
在全球竞速中,中国的科研力量不容小觑。国内多家生物科技公司和研究机构正积极布局mRNA肿瘤疫苗的研发。
LK101注射液数据亮眼
国产LK101注射液在肝细胞癌的临床研究中表现卓越,接种疫苗组患者2年生存率达到100%,所有12名患者生存期均超过4年。这标志着中国患者无需远渡重洋,就能接触到国际同步的尖端治疗。
R01疫苗:胰腺癌与消化系统肿瘤的潜力
2月11日,杭州纽安津生物技术有限公司自主研发的个体化肿瘤新生抗原mRNA疫苗R01注射液,正式获得国家药品监督管理局(NMPA)的临床试验默示许可。
2025年癌症免疫治疗学会(SITC)年会上公布的临床研究结果显示:在晚期胰腺癌一线治疗中,1例完全缓解(CR),3例部分缓解(PR),其余均为疾病稳定(SD),中位无进展生存期(PFS)达14.9个月,中位总生存期(OS)达19.7个月,12个月无进展生存率51.6%,12个月总生存率88.9%。
在标准治疗失败的晚期末线消化系统恶性肿瘤患者中,R01同样展现出潜力。临床研究结果显示:中位OS为9.3个月,12个月生存率44.4%。这些数据超过了传统二线及三线标准治疗的历史表现,为那些几乎耗尽所有治疗选择的患者提供了新的可能性。
目前,mRNA癌症疫苗主要应用于临床试验阶段,未正式上市。是否适合,取决于癌症类型、基因突变特征、既往治疗史等多重因素,需要由专业团队进行全面评估。
结语
mRNA癌症疫苗代表了肿瘤免疫治疗的一个极具前景的方向,但它并非“万能神药”。它的兴起,让我们看到了利用人体自身免疫系统战胜癌症的更多可能。然而,从振奋人心的临床数据到成为每位患者触手可及的治疗选择,仍有很长的路要走。但个体化mRNA疫苗等创新疗法,已经让我们看到了将癌症转变为一种可长期控制、甚至治愈的疾病的真实可能性。
未来,随着更多临床数据的积累、技术工艺的优化以及监管路径的明晰,个性化癌症疫苗有望逐步从前沿探索走向临床普及,为更多患者提供更有效、更精准的治疗选择。