是系统整体的能量度量,包含了内能和熵的贡献,主要用于判断反应的自发性。是分子与固体表面之间相互作用的能量变化,主要关注的是局部的吸附过程。想象一下,你有一杯水放在桌子上。这杯水看起来安安静静的,对吧?但在微观世界里,水分子们可“躁动”着呢!自由能(常用G表示)它融合了系统内部的能量(热力学能U)、混乱度(熵S)以及所处的环境(温度T、压力P)信息。
能做多少功?自由能的降低量 (-ΔG) 直接告诉你,这个系统在特定条件下(通常是恒温恒压),最多能对外做多少非体积功(比如电功、机械功)。就像你口袋里的钱,减少的钱数(ΔG)代表你能买多少东西(对外做功)。变化往哪走?ΔG是判断一个过程(比如冰融化、铁生锈、分子吸附到表面) 能不能自发进行的黄金标准:
ΔG > 0:过程不能自发进行。你要想让它发生,就得从外界输入能量“推”它一把(比如充电才能电解水)。这是“上坡”过程。
稳定性的标尺:自由能越低,系统通常越稳定。就像水往低处流,系统也“追求”更低自由能的状态。
这个名字不是所有能量都能随便用的(比如分子无规则热运动的动能,就很难有效利用),G 代表的就是“可利用”的部分。
如果一个坐标图,纵轴是自由能,横轴是“反应坐标”或“系统状态”。 初始状态 (比如干净的催化剂表面 Clean) 在某个高点G_initial。
曲线的高度差就代表了过程释放的能量大小。

10.1016/j.jcis.2023.10.058
另一张图,是同时,这张图完美展示了系统如何通过调整结构(优化)达到最低自由能(最稳定吸附态)的过程。
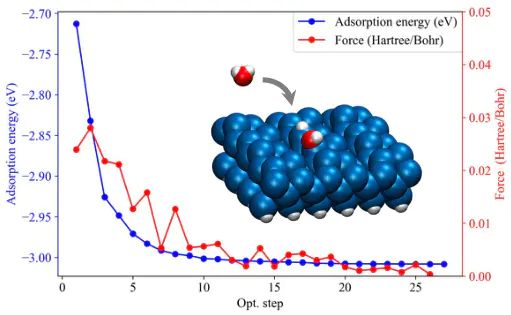
吸附能
AdsorptionAdsorption Energy, E_ads就是这个特定吸附过程导致的(ΔG_ads)更严格地说,它通常指在特定条件下(温度、压力),一个吸附质分子(或原子、离子)从自由状态(比如气相)跑到吸附剂表面固定位置并稳定下来,这个过程引起的系统能量的变化。
吸附有多“爽”?E_ads 的大小和符号直接告诉你吸附过程有多“自发”和有多“牢”。
通常是很大的负数):强烈自发!自由能大幅降低,吸附质“死心塌地”地粘在表面,结合非常牢固。数值越负(比如-2.0eV比-1.0eV),结合越强,越难脱附(掉下来)。
正值):不自发!自由能升高了,吸附质“不喜欢”这个表面,要么粘不上,要么粘上了也容易跑掉。
:脱附平衡。
PhysisorptionChemisorption(E_ads范德华化学吸附通常在-1eV到-10eV):吸附质和吸附剂表面原子之间发生了电子共享或转移,形成了(共价键、离子键、配位键等)。就像把纸焊(化学键)在铁板上。
H*催化活性的“晴雨表”:在催化领域,吸附能是核心描述符!一个理想的催化剂,需要恰到好处地吸附反应物分子(太弱吸不住,太强又“勒死”了反应物让它反应不了),然后让它在表面反应后产物能顺利脱附(脱附也需要能量,脱附能太大也不行)。
材料设计的指南针:知道目标分子在某种材料表面的吸附能,就能预测这种材料是否适合做吸附剂(如污水处理、气体分离)、催化剂、传感器、电池电极材料等。科学家们通过计算模拟(或实验测量,不断寻找具有理想吸附能的新材料。
实际应用
(VOCs化工生产催化剂):合成氨、炼油、汽车尾气净化都离不开催化剂。原料气体分子(如)必须先吸附到催化剂表面(如Fe, Pt, Pd),才能被打断化学键、重组形成新分子(NH₃, 汽油组分, CO₂/N₂)。原料分子吸附太弱(E_ads>0或小负值),抓不住分子;吸附太强(E_ads很负),反应完了产物也下不来,催化剂“中毒”。寻找E_ads刚刚好的催化剂(火山顶)是关键!。
(浮选选矿界面吸附):塑料浮选、铁矿浮选都依赖药剂选择性吸附在特定矿物表面,改变其亲水性疏水性。捕收剂在有用矿物表面吸附能要强(化学吸附居多),让它疏水上浮;在脉石矿物表面吸附能要弱。起泡剂在气液界面吸附能要适中。所有界面相互作用(固/液、液/气、固/气)的核心都是自由能最小化驱动。
总结
(G)(E_ads)它专注于记录一个分子(吸附质)和一个表面(吸附剂)结合时,整个系统“总账本”发生了多少变化(通常是亏钱变富,ΔG)。吸附能是自由能变化的一种具体体现和应用。理解了自由能,就理解了吸附能的理论根基;理解了吸附能,就看到了自由能如何在界面科学、催化、材料等领域大显身手。
状态函数的变化量